-

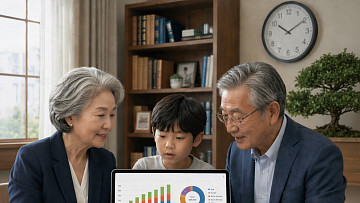
- “곧 나온다더니…” 꿈의 약 치매치료제, 현실에선 언제?
- 치매치료제들은 이름부터 어렵다. 게다가 성분명까지 함께 거론되니 일반 소비자 입장에선 더욱 헷갈리기 마련이다. 그 어려운 이름 중 우리의 가슴을 설레게 했던 최초의 치매치료제 아두헬름(성분명 아두카누맙)은 올해 1월 시장에서 사라졌다. 환자들의 기대와 달리 부작용 등 고전을 면치 못했기 때문이다. 그렇다면 희망은 사라진 것일까. 결론부터 말하자면
- 2024-09-11 08:27
-

- 전문가가 바라본 알츠하이머성 치매 연구 조작의 전말
- 최근 바이오젠의 아두카누맙을 필두로 치매 치료제 개발에 대한 희소식이 들려오고 있는 가운데, 놀라운 소식이 하나 전해졌다. 바로 치매 연구의 ‘근간’이라 평가받는 미네소타대학 연구팀의 논문 ‘조작설’이다. 치매 치료제를 손꼽아 기다리고 있는 독자들을 위해 전문가에게 이 사건의 전말과 앞으로의 영향에 대해 들어보았다. - 편집자 주 - 치매는
- 2022-10-14 09:01
-
- 치매 치료제 개발 눈앞 “신약이 보인다”
- 바이오 산업 분야에서 치매 치료제는 ‘대박’이 확실한 흥행 보증수표다. 국제알츠하이머병기구는 세계 치매 환자 수가 2030년 7600만 명을 넘고, 2050년에는 1억 3500만 명에 이를 것으로 전망했다. 제약회사들은 이 시장을 보고 개발에 뛰어들고 있다. 하지만 일반인이 모르는 부분이 있다. 이 회사들 중 99%는 뇌기능의 회복이 아니라, 발병한 치매를
- 2022-04-04 09:39
-

- 치매 속도 늦추는 치료제, 미 FDA 신약 첫 승인
- 노인 10명 중 1명이 앓고 있는 치매 속도를 늦추는 치료제가 처음으로 승인받았다. 미국 식품의약국(FDA)은 7일(현지 시간) 미국 벤처기업 바이오젠과 일본 에자이가 공동으로 개발한 알츠하이머 치료제인 '아두카누맙'을 조건부로 승인했다. 임상시험에서 기억력을 떨어뜨리는 속도를 늦추는 효과를 입증했지만 효능과 안전성을 확인하는 임상4상 시험을 통과
- 2021-06-09 14:50
이투데이
-
- ‘아밀로이드 베타 제거’ 소용없나…치매 치료제 개발 현주소는
- 알츠하이머성 치매 치료제 개발 기업들이 다양한 기전을 탐색할 필요성이 커지고 있다. 기존의 아밀로이드 베타 단백빌 제거 기전 중심에서 염증 억제, 신경세포 보호 등 다양한 메커니즘으로 패러다임을 전환해야 한다는 것이 학계 의견이다. 이에 국내외 제약바이오 업계의 치매 치료제 연구개발(R&D) 동향이 바뀔지 관심이 쏠린다. 26일 제약바이오 업계에 따르
- 2026-04-27 05:00
-

- J&J·노보노디스크도 실패…알츠하이머병 치료제 개발 난항
- 글로벌 제약사들이 잇따라 알츠하이머병 치료제 개발 실패를 발표했다. 미국 존슨앤드존슨(J&J)과 덴마크 노보노디스크가 임상에서 의미 있는 효과를 입증하지 못하며 연구 중단 또는 방향 전환에 나서면서 알츠하이머병 치료제 개발의 어려움이 재차 부각하고 있다. 25일 제약바이오업계에 따르면 노보노디스크는 ‘위고비’란 제품명으로 잘 알려진 비만·당뇨 치료제 ‘
- 2025-11-26 05:00
-
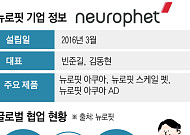
- 로슈·릴리가 선택한 뉴로핏, AI로 알츠하이머 진단·CRO 시장 겨눈다
- 레켐비·키순라 등 치료제 연이어 FDA 허가알츠하이머 진단·부작용 관리 중요성 커져뉴로핏, PET·MRI 기반 AI 분석으로 승부 최근 알츠하이머병 치료제가 잇달아 미국 식품의약국(FDA) 승인을 받으며 퇴행성 뇌질환 치료제 시장이 주목받고 있다. 이에 따라 치료를 넘어 진단과 부작용 관리 등 뇌질환 전주기를 아우르는 기술의 중요성이 커지고 있다. 인공
- 2025-07-31 05:00